Unterschied zwischen Veresterung und Umesterung
 Share
Share
Hauptunterschied - Veresterung vs. Umesterung
Veresterung und Umesterung sind zwei mit Estern verwandte Begriffe. Ester sind chemische Verbindungen, die von einer Säure abgeleitet wurden, indem ihre -OH-Gruppe durch eine Alkoxygruppe ersetzt wurde. Ester werden typischerweise aus Carbonsäuren gebildet. Sie sind polare Moleküle und können aufgrund der Anwesenheit von Sauerstoffatomen Wasserstoffbrückenbindungen mit anderen Molekülen eingehen. Veresterung ist das Verfahren zur Herstellung eines Esters. Umesterung ist die Modifikation von Estern durch chemische Reaktionen. Der Hauptunterschied zwischen Veresterung und Umesterung ist der Veresterung schließt einen Ester als Endprodukt ein, während die Umesterung einen Ester als Reaktanten einschließt.
Wichtige Bereiche
1. Was ist Veresterung?
- Definition, Mechanismus, Beispiele
2. Was ist Umesterung?
- Definition, Mechanismus, Beispiele
3. Was ist der Unterschied zwischen Veresterung und Umesterung
- Vergleich der wichtigsten Unterschiede
Schlüsselbegriffe: Alkohol, Alkoxygruppe, Carbonsäuren, Veresterung, Ester, Umesterung
Was ist Veresterung?
Veresterung ist der Prozess, bei dem ein Ester gebildet wird. Meist wird dies mit Carbonsäuren durchgeführt. Veresterung tritt auf, wenn eine Carbonsäure mit einem Alkohol reagiert. Diese Reaktion ist nur möglich, wenn dem Reaktionsgemisch ein saurer Katalysator und Wärme zugeführt werden. Ansonsten findet keine Reaktion statt, auch wenn Carbonsäure und Alkohol miteinander vermischt werden. Dies liegt daran, dass dieses Verfahren eine hohe Energie benötigt, um die -OH-Gruppe von der Carbonsäure zu entfernen. Daher wird ein Katalysator benötigt, um die Aktivierungsenergie der Reaktion zu reduzieren, und als Energiequelle wird Wärme benötigt.
Das bei dieser Reaktion gebildete Nebenprodukt ist Wasser. Daher können wir in Gegenwart eines Dehydratisierungsmittels das reine Esterprodukt erhalten. Durch Veränderung der Carbonsäure oder des Alkohols kann der Ester mit den gewünschten Kohlenstoffatomen erhalten werden. Die Veresterungsreaktion ist eine Gleichgewichtsreaktion. Um eine hohe Ausbeute an Ester zu erhalten, können wir entweder eine überschüssige Menge Alkohol oder ein Dehydratisierungsmittel verwenden, um Wasser aus dem System zu entfernen. Wenn nicht, kann Wasser durch andere Verfahren wie Destillation entfernt werden.

Abbildung 01: Synthese von Methylacetat
Das obige Bild zeigt die Herstellung von Methylacetat unter Verwendung von Ethansäure und Methanol als Reaktanten. Das Nebenprodukt ist ein Wassermolekül. Das Wassermolekül wird aus dem H gebildet+ kommt aus Alkohol und der -OH der Carbonsäure. Der hier verwendete Katalysator ist Schwefelsäure.
Was ist Umesterung?
Umesterung ist der Austausch der Alkylgruppe, die an das Sauerstoffatom des Esters gebunden ist, mit der Alkylgruppe eines Alkohols. Diese Reaktion erfordert saure oder basische Katalysatoren, um die Aktivierungsenergie der Reaktion zu reduzieren.
Mechanismus
Die Umesterung eines Esters wird mit dem nucleophilen Angriff des Alkohols eingeleitet. Der Alkohol, der das an das Sauerstoffatom gebundene Proton entfernt, wird aufgrund der Anwesenheit von einsamen Elektronenpaaren zu einem Nucleophil. Dieses Nukleophil kann das Kohlenstoffatom angreifen, das an den zwei Sauerstoffatomen gebunden ist. Das Kohlenstoffatom wird partiell positiv geladen, da die beiden Sauerstoffatome die Bindungselektronen zu sich ziehen, da die Elektronenaffinität der Sauerstoffatome höher ist als die des Kohlenstoffatoms. Somit ist dieser Kohlenstoff mit der partiell positiven Ladung ein guter Angriffspunkt für das Nukleophil.
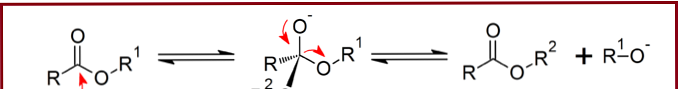
- Abbildung 02: Umesterungsreaktion
Dies bildet ein Zwischenmolekül, das aus Ester und Alkohol besteht, der durch seinen Sauerstoff an das Kohlenstoffatom (mit partiell positiver Ladung) gebunden ist. Da dieses Zwischenprodukt instabil ist, findet eine Neuanordnung statt. Dort wird die -OR-Gruppe der Carbonsäure entfernt. Die Alkoholgruppe bleibt jedoch an den Kohlenstoff gebunden. Nun entsteht ein neuer Ester.
Dieser Mechanismus wird in der Polyesterproduktion eingesetzt.
Unterschied zwischen Veresterung und Umesterung
Definition
Veresterung: Veresterung ist der Prozess, bei dem ein Ester gebildet wird.
Umesterung: Umesterung ist der Austausch der Alkylgruppe, die an das Sauerstoffatom des Esters gebunden ist, mit der Alkylgruppe eines Alkohols.
Ester
Veresterung: Der Ester ist das Endprodukt der Veresterung.
Umesterung: Der Ester ist ein Reaktant der Umesterung.
Nebenprodukt
Veresterung: Das Nebenprodukt der Veresterung ist ein Wassermolekül.
Umesterung: Das Nebenprodukt der Umesterung ist ein Nukleophil / Alkohol-Molekül.
Katalysator
Veresterung: Die Veresterung erfordert einen sauren Katalysator.
Umesterung: Die Umesterung erfordert saure oder basische Katalysatoren oder Enzyme.
Energiebedarf
Veresterung: Die Veresterung erfordert Wärmeenergie, um den Ester herzustellen.
Umesterung: Umesterung erfordert keine Wärme.
Fazit
Veresterung ist der Prozess, bei dem ein Ester gebildet wird. Umesterung ist der Prozess, bei dem ein Ester modifiziert wird. Der durch die Veresterung erzeugte Ester kann von der Umesterung abgeändert werden, um den gewünschten Ester zu erhalten. Der Hauptunterschied zwischen Veresterung und Umesterung besteht darin, dass die Veresterung einen Ester als Endprodukt einschließt, während die Umesterung einen Ester als Reaktanten einschließt.
Verweise:
1. "Veresterung: Definition, Prozess und Reaktionen." Study.com. Study.com, n.d. Netz. Hier verfügbar. 04 Aug. 2017.
2. "Umesterung". Wikipedia. Wikimedia Foundation, 01 Aug. 2017. Web. Hier verfügbar. 04 Aug. 2017.
Bildhöflichkeit:
1. "Veresterung (Essigsäure und Methanol)" von Doxepine - Eigene Arbeit, Public Domain) über Commons Wikimedia
2. "Allgemeiner Umesterungsmechanismus" von Rifleman 82 - Eigene Arbeit (Public Domain) über Commons Wikimedia

